La tabla periódica es uno de los pilares fundamentales de la química, un recurso que organiza y clasifica los elementos químicos de una manera que revela su comportamiento y propiedades. Pero, ¿alguna vez te has preguntado dónde se encuentra el número atómico en la tabla periódica? Esta consulta es más común de lo que piensas y es crucial para comprender la estructura y las características de los elementos. En este artículo, exploraremos en detalle el concepto de número atómico, su ubicación en la tabla periódica y su importancia en la química. Además, desglosaremos cómo interpretar esta información para que puedas utilizarla de manera efectiva en tus estudios o en cualquier contexto que lo requiera. Prepárate para adentrarte en el fascinante mundo de la química y descubrir la relevancia del número atómico.
¿Qué es el Número Atómico?
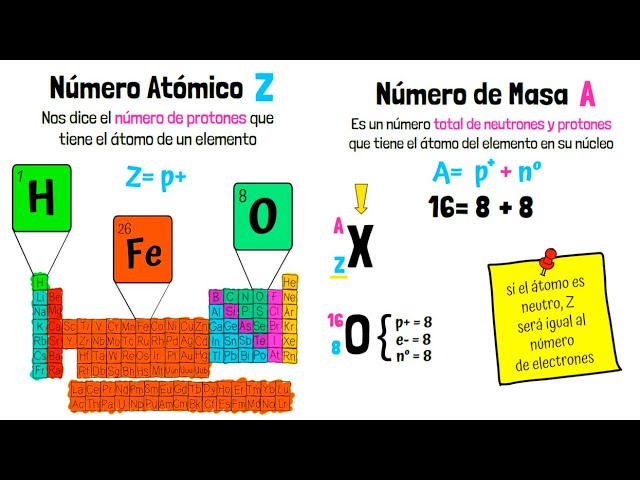
El número atómico es una propiedad fundamental de los elementos químicos que se representa con la letra «Z». Este número indica la cantidad de protones que se encuentran en el núcleo de un átomo. Dado que el número de protones determina las propiedades químicas y físicas de un elemento, el número atómico es esencial para la clasificación de los elementos en la tabla periódica.
1 Definición y Significado
Definir el número atómico como el número de protones en el núcleo de un átomo es solo el comienzo. Este número también influye en la carga eléctrica del átomo, ya que en un estado neutro, el número de electrones será igual al número atómico. Por ejemplo, el hidrógeno tiene un número atómico de 1, lo que significa que tiene un protón y, por lo tanto, un electrón. Esta relación es crucial para entender la estructura atómica y cómo los elementos interactúan entre sí.
2 Relación con los Isótopos
Es importante mencionar que el número atómico se distingue del número de masa, que es la suma de protones y neutrones en el núcleo. Los isótopos son variantes de un mismo elemento que tienen el mismo número atómico pero diferente número de neutrones. Por ejemplo, el carbono tiene un número atómico de 6, pero puede existir como carbono-12 o carbono-14, dependiendo de la cantidad de neutrones. Esto es esencial en campos como la datación por carbono y la medicina nuclear.
Localización del Número Atómico en la Tabla Periódica
Ahora que hemos establecido qué es el número atómico, es hora de descubrir dónde se encuentra en la tabla periódica. La tabla está organizada de manera que cada elemento ocupa un lugar específico, y el número atómico es una de las características más visibles y esenciales de cada elemento.
1 Diseño de la Tabla Periódica
La tabla periódica está compuesta por filas horizontales llamadas periodos y columnas verticales llamadas grupos. Cada casilla en la tabla representa un elemento y, generalmente, incluye su símbolo químico, su nombre y su número atómico. El número atómico se encuentra en la parte superior de cada casilla, a la izquierda del símbolo del elemento. Por ejemplo, el número atómico del oxígeno (O) es 8, lo que significa que tiene 8 protones en su núcleo.
2 Ejemplo de Interpretación
Para ilustrar esto, tomemos el elemento carbono (C). En la tabla periódica, el número atómico del carbono es 6, lo que indica que tiene 6 protones. Al observar la tabla, verás que el número atómico está siempre en la misma posición, lo que facilita la búsqueda de información sobre un elemento específico. Esto es especialmente útil cuando se estudian las propiedades y comportamientos de diferentes elementos en química.
Importancia del Número Atómico en la Química
El número atómico no solo es un dato numérico; tiene un impacto significativo en la química y en cómo entendemos el mundo que nos rodea. A continuación, exploraremos algunas de las razones por las que el número atómico es fundamental.
1 Identificación de Elementos
Una de las funciones más importantes del número atómico es la identificación de elementos. Cada elemento en la tabla periódica tiene un número atómico único, lo que significa que no hay dos elementos con el mismo número. Esta unicidad es esencial para la química, ya que permite a los científicos y estudiantes distinguir entre diferentes elementos y estudiar sus propiedades específicas.
2 Determinación de Propiedades Químicas
El número atómico también está relacionado con las propiedades químicas de un elemento. Por ejemplo, los elementos en el mismo grupo (columna) de la tabla periódica tienen propiedades similares debido a que tienen el mismo número de electrones en su capa más externa. Esto influye en cómo los elementos reaccionan entre sí. Por ejemplo, el sodio (Na) y el potasio (K) tienen números atómicos de 11 y 19, respectivamente, y ambos son metales alcalinos que reaccionan de manera similar con el agua.
Ejemplos de Elementos y sus Números Atómicos
Para entender mejor cómo se utiliza el número atómico en la práctica, examinemos algunos ejemplos de elementos comunes y sus números atómicos. Esto no solo te ayudará a familiarizarte con la tabla periódica, sino que también te permitirá ver cómo se relacionan estos números con las propiedades de los elementos.
1 Hidrógeno (H)
El hidrógeno, con un número atómico de 1, es el elemento más ligero y el más abundante en el universo. Es un gas incoloro y altamente reactivo que juega un papel crucial en la formación de compuestos, como el agua (H₂O). Su número atómico bajo significa que tiene un solo protón y un solo electrón, lo que lo convierte en un elemento simple pero fundamental.
2 Hierro (Fe)
El hierro, con un número atómico de 26, es un metal que se utiliza ampliamente en la construcción y la fabricación. Su capacidad para formar aleaciones y su resistencia a la corrosión lo hacen invaluable en la industria. Además, el hierro es esencial para la vida, ya que forma parte de la hemoglobina en la sangre, que transporta oxígeno a través del cuerpo.
Cómo Usar el Número Atómico en Problemas Químicos
Conocer el número atómico es fundamental no solo para la identificación de elementos, sino también para resolver problemas químicos. A continuación, veremos cómo se aplica en diferentes contextos.
1 Cálculos de Masa Molar
La masa molar de un elemento se puede calcular utilizando su número atómico. Por ejemplo, el carbono tiene un número atómico de 6 y una masa molar aproximada de 12 g/mol. Esto significa que un mol de átomos de carbono pesa aproximadamente 12 gramos. Esta información es esencial para realizar cálculos en química, como determinar la cantidad de reactivos necesarios en una reacción química.
2 Balanceo de Ecuaciones Químicas
El número atómico también juega un papel en el balanceo de ecuaciones químicas. Cuando se llevan a cabo reacciones químicas, es importante que la cantidad de átomos de cada elemento sea la misma en ambos lados de la ecuación. Conocer el número atómico ayuda a identificar cuántos átomos de cada elemento están presentes, lo que facilita el balanceo adecuado de la ecuación.
Avances Recientes en la Investigación de Elementos
La química es una ciencia en constante evolución, y la investigación sobre los elementos y sus propiedades sigue avanzando. A medida que se descubren nuevos elementos y se estudian sus características, el número atómico sigue siendo una herramienta clave para los científicos.
1 Nuevos Elementos en la Tabla Periódica
En los últimos años, se han añadido nuevos elementos a la tabla periódica, como el nihonio (Nh) y el moscovio (Mc). Cada uno de estos elementos tiene un número atómico único y se han sintetizado en laboratorios mediante reacciones nucleares. La investigación en estos elementos ayuda a comprender mejor la estructura del núcleo atómico y las fuerzas que lo mantienen unido.
2 Aplicaciones Prácticas en la Tecnología
Los avances en la comprensión de los elementos y sus números atómicos también han llevado a aplicaciones tecnológicas innovadoras. Por ejemplo, el desarrollo de materiales con propiedades específicas, como superconductores y semiconductores, se basa en la manipulación de los elementos a nivel atómico. Esto ha revolucionado la electrónica y la tecnología de materiales, mostrando la relevancia continua del número atómico en la ciencia moderna.
¿Qué es el número atómico y cómo se representa?
El número atómico es el número que indica la cantidad de protones en el núcleo de un átomo y se representa con la letra «Z». Este número es fundamental para identificar elementos en la tabla periódica y determina sus propiedades químicas.
¿Dónde se encuentra el número atómico en la tabla periódica?
En la tabla periódica, el número atómico se encuentra en la parte superior de cada casilla del elemento, generalmente a la izquierda del símbolo químico. Esta posición es constante para todos los elementos y facilita su identificación.
¿Cómo se relaciona el número atómico con los isótopos?
El número atómico se refiere a la cantidad de protones en un átomo, mientras que los isótopos son variantes de un elemento que tienen el mismo número atómico pero diferente número de neutrones. Esto significa que, aunque comparten el mismo número atómico, pueden tener diferentes propiedades físicas.
¿Por qué es importante el número atómico en la química?
El número atómico es crucial porque permite identificar elementos, determinar sus propiedades químicas y realizar cálculos en química, como la masa molar y el balanceo de ecuaciones. Sin esta información, sería difícil entender las interacciones entre los diferentes elementos.
¿Cómo afecta el número atómico a las propiedades de un elemento?
El número atómico influye en las propiedades químicas y físicas de un elemento, ya que determina la cantidad de electrones y protones. Esto afecta la reactividad, la formación de compuestos y otras características esenciales que son importantes en química.
¿Qué elementos tienen un número atómico más alto?
Los elementos con números atómicos más altos son aquellos que se encuentran al final de la tabla periódica. Estos incluyen elementos como el oganesón (Og) con un número atómico de 118. Muchos de estos elementos son sintéticos y tienen propiedades poco conocidas debido a su inestabilidad.
¿Cómo se utiliza el número atómico en la educación química?
El número atómico se utiliza en la educación química para enseñar a los estudiantes sobre la estructura atómica, la clasificación de elementos y la importancia de las propiedades químicas. Es un concepto básico que se aplica en numerosos contextos dentro del estudio de la química.