La tabla periódica es una de las herramientas más fundamentales en el estudio de la química, y uno de sus elementos más intrigantes es el número de masa. Pero, ¿qué es exactamente el número de masa y por qué es tan importante? En este artículo, te llevaremos a través de un viaje informativo que desentrañará todos los aspectos del número de masa. Desde su definición y cálculo, hasta su relevancia en diferentes campos de la ciencia, te proporcionaremos un panorama completo. Al final, tendrás una comprensión clara de cómo este concepto se entrelaza con la estructura de la materia y su aplicación en la vida cotidiana. Prepárate para descubrir todo lo que necesitas saber sobre el número de masa en la tabla periódica.
¿Qué es el Número de Masa?
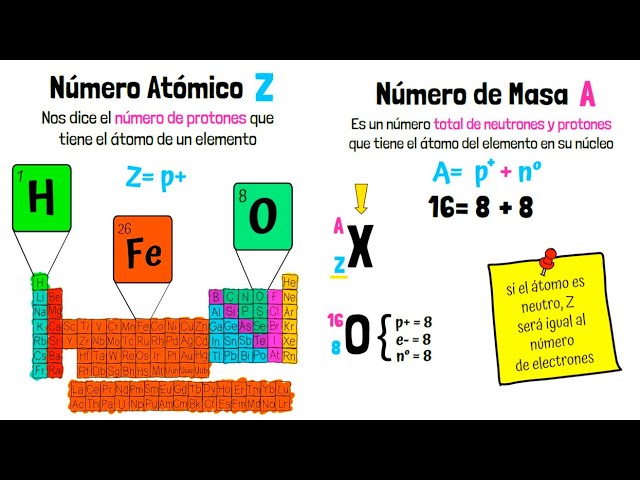
El número de masa es una propiedad fundamental de los átomos que se refiere a la suma total de protones y neutrones en el núcleo de un átomo. Este número se expresa como un número entero y es crucial para identificar el isótopo específico de un elemento. Por ejemplo, el carbono tiene un número atómico de 6, lo que significa que tiene 6 protones. Sin embargo, su número de masa puede variar dependiendo de la cantidad de neutrones presentes en el núcleo.
Protones y Neutrones: Los Componentes del Número de Masa
Para entender el número de masa, primero debemos explorar los componentes que lo conforman: los protones y los neutrones. Los protones son partículas subatómicas con carga positiva que determinan la identidad del elemento, mientras que los neutrones son partículas sin carga que contribuyen a la masa del núcleo.
- Protones: Cada elemento tiene un número específico de protones. Por ejemplo, el oxígeno tiene 8 protones, lo que lo clasifica como el elemento 8 en la tabla periódica.
- Neutrones: La cantidad de neutrones puede variar, dando lugar a isótopos. Por ejemplo, el carbono-12 tiene 6 neutrones, mientras que el carbono-14 tiene 8 neutrones.
Esta variabilidad en el número de neutrones es lo que permite que los elementos tengan diferentes isótopos, los cuales pueden tener propiedades químicas similares pero diferentes propiedades físicas, como la estabilidad nuclear.
¿Cómo se Calcula el Número de Masa?
Calcular el número de masa es un proceso relativamente sencillo. Se suma el número de protones y neutrones en el núcleo del átomo. Este número no se encuentra directamente en la tabla periódica, pero se puede deducir fácilmente si conoces el número atómico y el número de neutrones. El número atómico, que se encuentra en la parte superior del símbolo del elemento, indica el número de protones.
Ejemplo de Cálculo del Número de Masa
Imaginemos que queremos calcular el número de masa del oxígeno. Sabemos que:
- El oxígeno tiene un número atómico de 8 (por lo tanto, tiene 8 protones).
- Los isótopos más comunes del oxígeno son el oxígeno-16 y el oxígeno-18, que tienen 8 y 10 neutrones respectivamente.
Para el oxígeno-16, el cálculo sería:
Número de masa = Protones + Neutrones = 8 + 8 = 16.
De manera similar, para el oxígeno-18:
Número de masa = 8 + 10 = 18.
Esto ilustra cómo el número de masa varía entre los isótopos de un mismo elemento y es clave para entender su comportamiento en reacciones químicas y nucleares.
La Importancia del Número de Masa en la Química
El número de masa no solo es una cifra en la tabla periódica; tiene profundas implicaciones en la química. Desde la identificación de isótopos hasta su papel en las reacciones nucleares, el número de masa es fundamental para comprender cómo interactúan los elementos.
Identificación de Isótopos
La identificación de isótopos es una de las aplicaciones más importantes del número de masa. Los isótopos pueden tener propiedades químicas similares, pero diferentes propiedades físicas. Por ejemplo, el carbono-12 y el carbono-14 son isótopos del carbono que se utilizan en datación radiométrica, lo que permite a los científicos determinar la edad de objetos antiguos.
Reacciones Nucleares y Energía
Además, el número de masa juega un papel crucial en las reacciones nucleares. En la fisión y fusión nuclear, los cambios en el número de masa de los núcleos atómicos son fundamentales para liberar energía. Por ejemplo, en la fisión del uranio, el núcleo se divide en núcleos más pequeños, y el número de masa total de los productos es menor que el del núcleo original, lo que resulta en la liberación de energía.
Diferencias entre Número de Masa y Número Atómico
Es común confundir el número de masa con el número atómico, pero hay diferencias clave entre ambos. El número atómico se refiere exclusivamente al número de protones en un átomo, mientras que el número de masa incluye tanto protones como neutrones.
Definiciones Claras
- Número Atómico: Número de protones en el núcleo de un átomo, que determina la identidad del elemento.
- Número de Masa: Suma de protones y neutrones en el núcleo, que indica la masa total del átomo.
Por ejemplo, el hidrógeno tiene un número atómico de 1 (1 protón) y un número de masa de 1 en su isótopo más común, el hidrógeno-1, que no tiene neutrones. Sin embargo, el hidrógeno tiene otros isótopos, como el deuterio (hidrógeno-2) y el tritio (hidrógeno-3), que tienen 1 y 2 neutrones respectivamente, lo que cambia su número de masa.
Aplicaciones del Número de Masa en la Vida Cotidiana
El número de masa no es solo un concepto teórico; tiene aplicaciones prácticas en diversas áreas de nuestra vida cotidiana. Desde la medicina hasta la industria, el número de masa es crucial para una variedad de procesos.
Medicina y Diagnóstico
En medicina, el número de masa es vital para la tomografía por emisión de positrones (PET), que utiliza isótopos radiactivos para diagnosticar enfermedades. Por ejemplo, el flúor-18 se utiliza en la PET para detectar tumores, ya que su número de masa permite que sea rastreado en el cuerpo humano.
Industria y Energía
En la industria, el número de masa es importante en la producción de materiales y en la comprensión de reacciones químicas. La energía nuclear, que depende de la fisión y fusión de núcleos atómicos, también se basa en el número de masa para calcular la energía liberada y gestionar la seguridad en plantas nucleares.
¿Por qué el número de masa es importante en la química?
El número de masa es crucial porque permite identificar isótopos de un elemento, que pueden tener diferentes propiedades físicas. Además, es fundamental en reacciones nucleares y en la comprensión de la estabilidad de los núcleos atómicos.
¿Cómo se relaciona el número de masa con la estabilidad de los isótopos?
La estabilidad de un isótopo está relacionada con la proporción de neutrones a protones. Isótopos con un número de masa muy alto pueden ser inestables y descomponerse, liberando radiación. La estabilidad es un factor clave en la datación y aplicaciones nucleares.
¿El número de masa siempre es un número entero?
Sí, el número de masa se expresa como un número entero porque representa la suma total de protones y neutrones. Sin embargo, en la tabla periódica, a veces se presenta un valor promedio que puede incluir decimales, lo que refleja la abundancia relativa de isótopos en la naturaleza.
¿Qué es un isótopo y cómo se relaciona con el número de masa?
Un isótopo es una variante de un elemento que tiene el mismo número de protones pero diferente número de neutrones, lo que cambia su número de masa. Por ejemplo, el carbono-12 y el carbono-14 son isótopos del carbono con números de masa diferentes.
¿Cómo se utiliza el número de masa en la medicina moderna?
En medicina, el número de masa es utilizado en técnicas como la tomografía por emisión de positrones (PET), donde isótopos radiactivos se utilizan para diagnosticar enfermedades. Estos isótopos tienen números de masa específicos que permiten su rastreo en el cuerpo.
¿El número de masa afecta las propiedades químicas de un elemento?
En general, el número de masa no afecta las propiedades químicas de un elemento, ya que estas dependen principalmente del número de electrones y la configuración electrónica. Sin embargo, los isótopos pueden tener diferentes propiedades físicas, como la densidad o la estabilidad.
¿Cómo se determina el número de masa en un laboratorio?
En un laboratorio, el número de masa se puede determinar utilizando espectrometría de masas, una técnica que permite medir la masa de los átomos y moléculas. Este método proporciona información precisa sobre la composición isotópica de una muestra y su número de masa correspondiente.